近日,中国农业科学院哈尔滨兽医研究所在解析非洲猪瘟病毒(ASFV)感染致病机制方面取得重要进展。研究发现,MGF300-4L蛋白为ASFV新的毒力相关因子并解析了其作用机制。相关研究成果于3月19日发表在《Emerging Microbes & Infections》杂志。
目前对于ASFV毒力相关因子及其作用机制的了解十分有限,制约了安全、有效疫苗的研发。猪烈性传染病创新团队前期研究提示,多基因家族基因(MGFs)与ASFV的致病性和其在靶细胞猪肺泡巨噬细胞(PAMs)中的复制密切相关。为探究调控ASFV在PAMs中复制的关键MGFs,研究人员创新性地采用MGFs大片段与单个基因缺失相结合的策略,成功鉴定出MGF300家族基因(1L、2R和4L)为ASFV在PAMs中复制降低的关键基因。进一步研究发现,MGF300-2R可招募自噬受体TOLLIP并通过选择性自噬降解IKKα和IKKβ,进而抑制NF-κB信号通路调控的炎性细胞因子IL-1β和TNF-α的产生,从而影响ASFV的致病性,表明其为ASFV的毒力相关因子(Wang et al., PLoS Pathogens, 2023)。
本研究发现,与MGF300-2R的作用机制不同,MGF300-4L可通过双靶标作用机制调控ASFV的致病性。研究表明,MGF300-4L与NF-κB信号通路中的关键分子IKKβ和IκBα均存在相互作用。一方面,MGF300-4L可招募HSC70并通过分子伴侣介导的自噬途径降解IKKβ;另一方面,MGF300-4L与IκBα的直接相互作用,抑制了E3泛素连接酶β-TrCP对IκBα的泛素化降解,增加了IκBα的稳定性,从而抑制了NF-κB信号通路调控的IL-1β和TNF-α的产生。体内感染试验显示,与野生型毒株(ASFV-WT)相比,接种102 TCID50的MGF300-4L基因缺失突变体病毒(Del4L),对猪的致死率降低50%,表明MGF300-4L为ASFV的毒力相关因子。深入分析发现,与ASFV-WT相比,Del4L在猪体内的复制显著降低并可以诱导高水平IL-1β和TNF-α的产生,同时可以激发良好的体液和细胞免疫应答。本研究不仅证实MGF300-4L为ASFV的毒力相关因子,也为ASF减毒活疫苗的科学设计提供了新靶标。
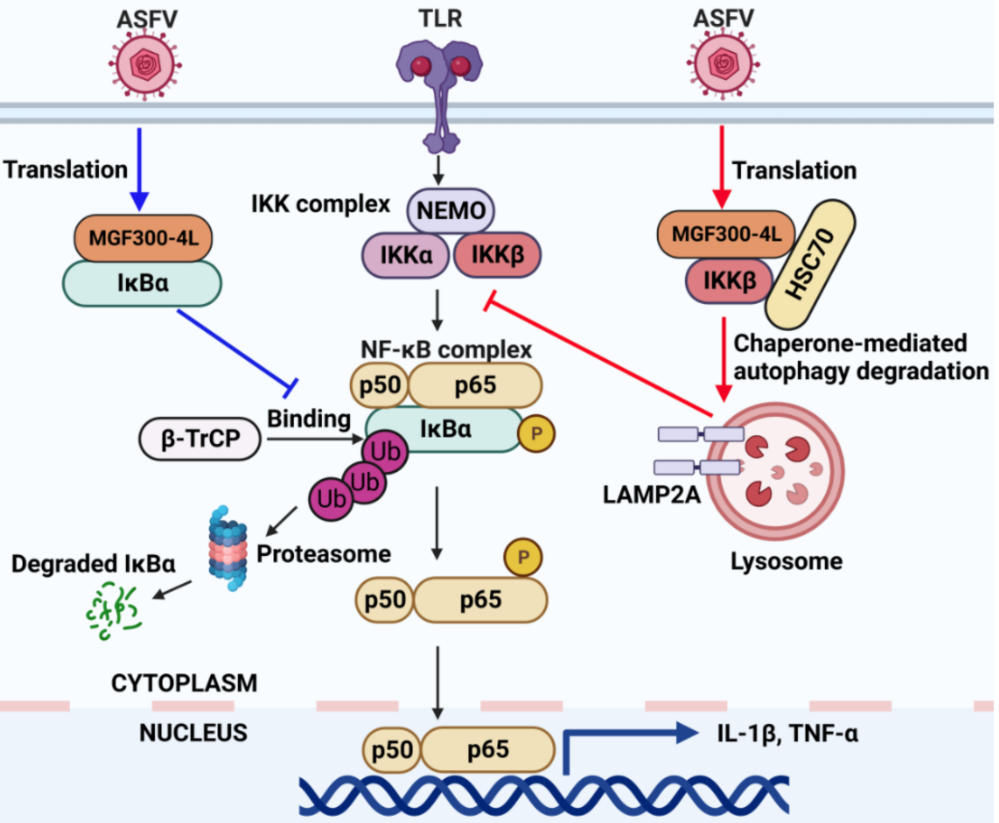
MGF300-4L蛋白作用机制示意图
本研究得到国家自然科学基金项目(32202774、32072854、U20A2060、32372983和32072855)的资助。中国农业科学院哈尔滨兽医研究所博士后王涛、博士研究生罗瑞和博士后张晶为文章的共同第一作者,仇华吉研究员、孙元研究员和李连峰副研究员为本文的共同通讯作者。
文章标题及链接:“The African swine fever virus MGF300-4L protein is associated with viral pathogenicity by promoting the autophagic degradation of IKKβ and increasing the stability of IκBα”,https://www.tandfonline.com/doi/full/10.1080/22221751.2024.2333381