近日,中国农业科学院哈尔滨兽医研究所揭示了E3泛素连接酶Stub1通过分子伴侣介导的自噬(CMA)途径选择性降解抗病毒关键激酶TBK1,从而负调控I型干扰素信号通路的全新机制,相关研究成果发表在《细胞死亡和分化(Cell Death & Differentiation)》上。
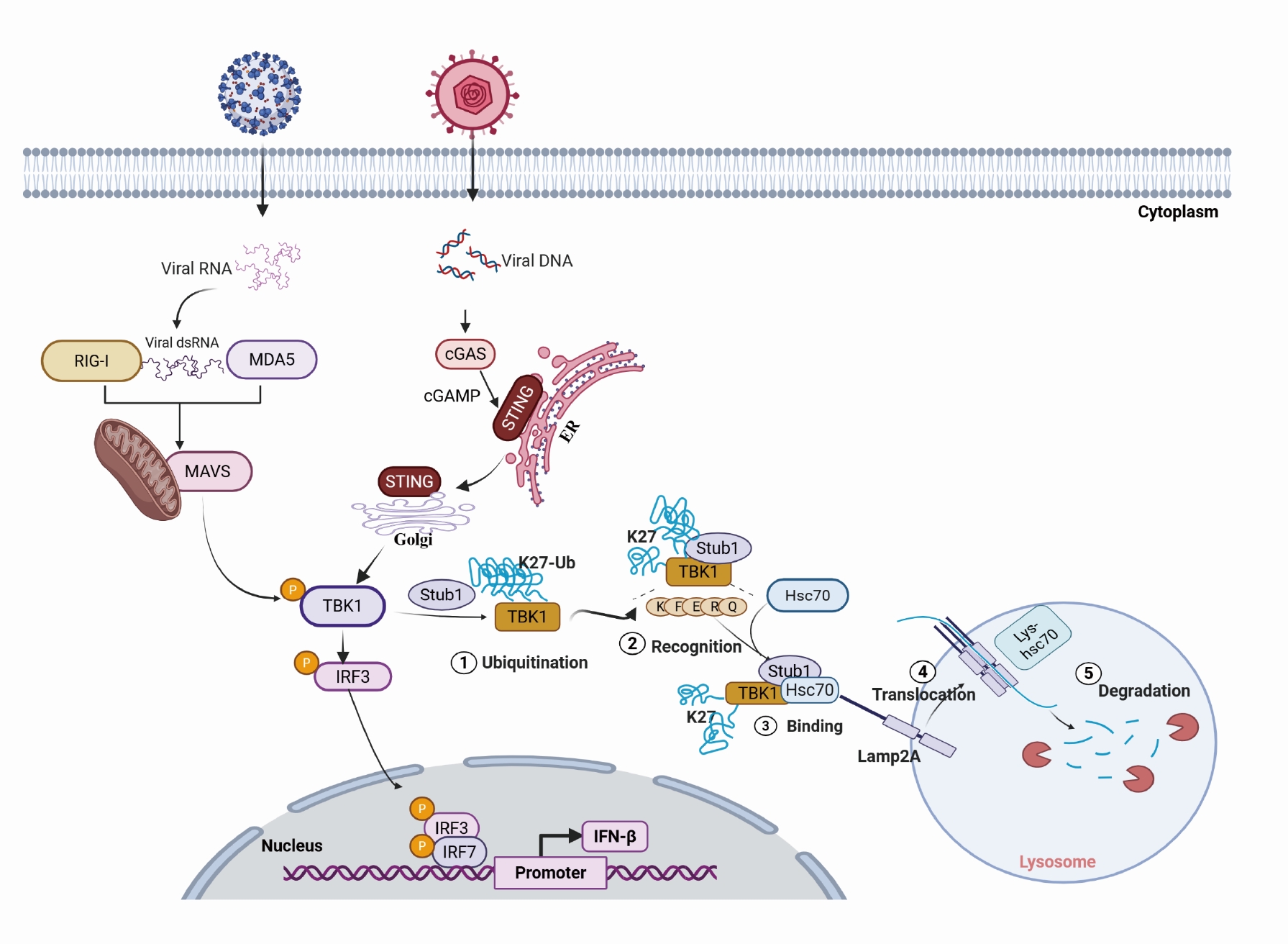
cGAS-STING及RIG-I-MAVS等先天免疫信号通路在宿主抵御病毒感染中发挥核心作用,其中,TBK1作为关键激酶,负责磷酸化IRF3并启动I型干扰素(如IFN-β)的表达,是抗病毒免疫的“枢纽”分子。TBK1的活性与稳定性受到多种翻译后修饰精细调控,但其如何被选择性降解以维持免疫稳态的机制尚不清晰。
该研究发现,E3泛素连接酶Stub1能直接结合TBK1,并通过其E3连接酶活性,在TBK1的K344位点催化K27多聚泛素化修饰。与传统的K48泛素化降解途径不同,该修饰使TBK1被分子伴侣蛋白HSC70识别,并通过CMA途径转运至溶酶体内降解,从而有效阻断I型干扰素的产生,促进病毒复制。本研究系统阐明了Stub1-TBK1轴在抗病毒免疫中的负向调控机制,将CMA途径与TBK1的稳定性调控直接关联,揭示了病毒感染过程中宿主利用CMA途径实现免疫“刹车”的精细平衡机制。
中国农业科学院哈尔滨兽医研究所基础免疫创新团队博士后刘宏扬为论文第一作者,翁长江研究员为通讯作者。该研究得到了国家自然科学基金的资助。
原文标题与链接:
”E3 ubiquitin ligase Stub1 enhances viral replication by promoting TBK1 degradation through molecular chaperone-mediated autophagy“
https://www.nature.com/articles/s41418-026-01716-7
上一篇:哈兽研阐明结核分枝杆菌PE_PGRS23蛋白抑制巨噬细胞自噬促进病原菌胞内存活的机制 下一篇:兽医学院与湖北金林共建研究生教育实践基地