近日,中国农业科学院哈尔滨兽医研究所与美国伊利诺伊大学合作,揭示了细胞内质网质量控制的固有抗病毒防御机制,相关研究成果发表在《前沿科学(Advanced Science)》杂志上。
细胞内质网是蛋白质合成和折叠的“工厂”,为了维持健康,细胞配备了一套严格的“质量控制系统”,负责清除错误折叠的蛋白质。传统意义上,这套系统被认为主要通过两种方式工作:一种是泛素蛋白酶体降解,另一种是自噬-溶酶体降解。
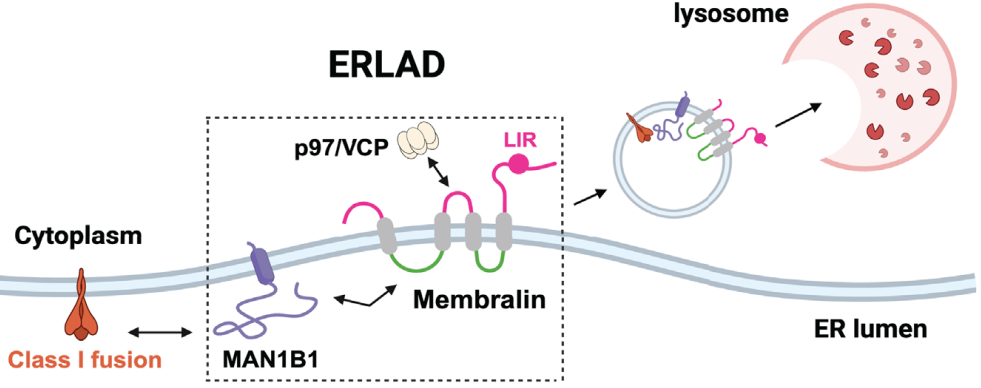
该研究发现,Membralin蛋白能够组建第三条、且具有高度选择性的销毁通路。当细胞自身的蛋白质发生错误折叠时,它们主要通过传统的两条路径被处理。然而,当病毒蛋白入侵时,Membralin复合体却被优先激活。它像一座桥梁,一端在内质网腔内“招募”糖基修剪酶MAN1B1,另一端在细胞质内“招募”分子马达VCP/p97,而其自身则带有一个能与自噬机器结合的“钩子”。这个由Membralin、MAN1B1和VCP组成的复合体,能够特异性地将多种致命病毒的表面糖蛋白——包括新冠病毒的S蛋白、埃博拉病毒的GP蛋白、流感病毒的HA蛋白以及HIV病毒的Env蛋白——运送至溶酶体进行销毁。该研究首次将Membralin定义为一种新型的“内质网自噬受体”,并完整解析了一条不依赖泛素化标记的内质网相关溶酶体降解通路,极大丰富了细胞生物学的基础认知,为开发针对多种包膜病毒的广谱治疗策略提供新靶点。
中国农业科学院哈尔滨兽医研究所张晶副研究员和博士研究生卢晓冉为论文共同第一作者,伊利诺伊大学郑永辉教授为通讯作者。该研究得到国家自然科学基金(32300129和32172836),中国农业科学院“青年创新专项”(Y2025QC19)和中国博士后科学基金(2023T160700)资助。
论文标题:Membralin Assembles a MAN1B1-VCP Complex to Target Foreign Glycoproteins from the Endoplasmic Reticulum to Lysosomes for Degradation
原文链接:https://pubmed.ncbi.nlm.nih.gov/41324484/