非洲猪瘟是由非洲猪瘟病毒感染猪引起的一种急性、高致死性传染病。该病自2018年传入我国,给我国养猪业带来了严重的经济损失。由于病毒感染和致病机制不清楚,而且缺乏商品化的疫苗和特效药物,非洲猪瘟的防控形势仍然异常严峻。因此,解析非洲猪瘟病毒感染和致病机制是当前迫切需要研究的科学问题。在中国农业科学院创新工程、国家自然科学基金委非洲猪瘟重点专项和兽医生物技术国家重点实验室课题的资助下,中国农业科学院哈尔滨兽医研究所青年科研人员,克服重重困难,在非洲猪瘟基础研究上取得一系列重要研究进展,为新型非洲猪瘟病毒减毒疫苗的研发提供了重要科学依据。
1. 揭示了非洲猪瘟病毒MGF505-7R基因与病毒致病力相关
发现和鉴定非洲猪瘟关键毒力基因是非洲猪瘟减毒活疫苗研发的基础。2021年7月26日,哈尔滨兽医研究所发现了一个非洲猪瘟病毒关键毒力基因,并在致病机制研究上取得新进展,相关研究结果以 “pMGF505-7R determines pathogenicity of African swine fever virus infection by inhibiting IL-1βand type I IFN production”为题,发表在《PLoS Pathogens》杂志上。该研究证实非洲猪瘟多基因家族蛋白pMGF505-7R与非洲猪瘟病毒的致病力密切相关。
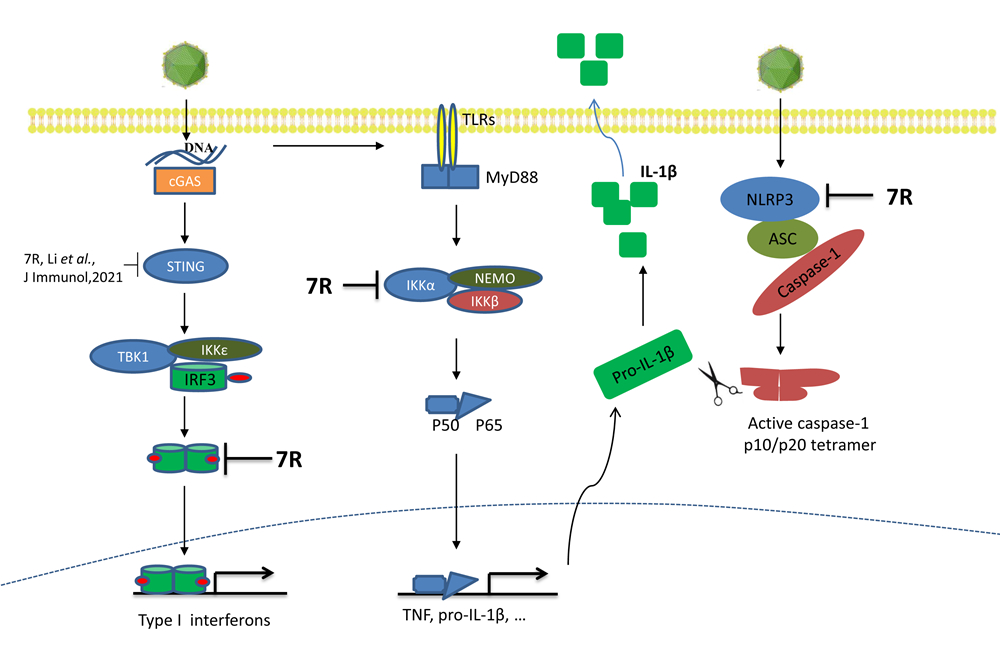
研究发现,非洲猪瘟病毒感染原代猪肺泡巨噬细胞能抑制多种刺激诱导的IL-1β和IFN-β的升高,提示非洲猪瘟病毒编码蛋白可能抑制IL-1β和IFN-β产生。通过筛选,研究人员发现非洲猪瘟病毒多基因家族(MGF)505/360多数成员对IL-1β和IFN-β产生具有抑制作用,其中pMGF505-7R的抑制作用最为显著。敲除MGF505-7R基因的重组病毒能够诱导更高水平的IL-1β和IFN-β的产生,表明pMGF505-7R对IL-1β和I型干扰素产生具有抑制作用。进一步研究发现pMGF505-7R通过与IKK复合物相互作用抑制IL-β基因的转录,并且其靶向NLRP3炎症复合体抑制IL-β的分泌。而在I型IFN信号通路中,pMGF505-7R靶向IRF3抑制I型IFN的产生。动物实验结果表明,缺失MGF505-7R基因的重组非洲猪瘟病毒对仔猪的致病力降低,感染猪血清中IL-1β和IFN-β的蛋白水平升高,而组织器官病毒载量显著降低。这些研究成果初步揭示了非洲猪瘟病毒的免疫逃逸的一种新策略,为非洲猪瘟病毒致病机制探索和疫苗的研发提供了新的理论依据。
2. 揭示了非洲猪瘟病毒免疫逃逸新的机制
非洲猪瘟病毒免疫逃逸机制与病毒的致病力和抗病毒猪的遗传育种密切相关。2021年11月10日,哈尔滨兽医研究所在非洲猪瘟病毒免疫逃逸机制研究上取得新进展,研究成果以 “African swine fever virus pI215L negatively regulates cGAS-STING signaling pathway through recruiting RNF138 to inhibit K63-linked ubiquitination of TBK1”为题,发表在《Journal of Immunology》杂志上,并被主编推荐为Top Read文章。该研究发现非洲猪瘟病毒编码的pI215L蛋白能够抑制Ⅰ型干扰素的产生,并阐明了该蛋白抑制Ⅰ型干扰素产生的分子机制。
先天免疫是宿主抵抗病原微生物感染的第一道防线,炎症反应和I型干扰素是先天免疫应答的重要成分,非洲猪瘟病毒感染如何逃逸宿主的先天免疫系统的监视,其与病毒致病力的关系尚不完全清楚。已有研究表明,ASFV拮抗干扰素(IFN)产生的基因与其致病力密切相关,缺失ASFV拮抗IFN产生的基因是研发ASFV疫苗的有效策略之一。
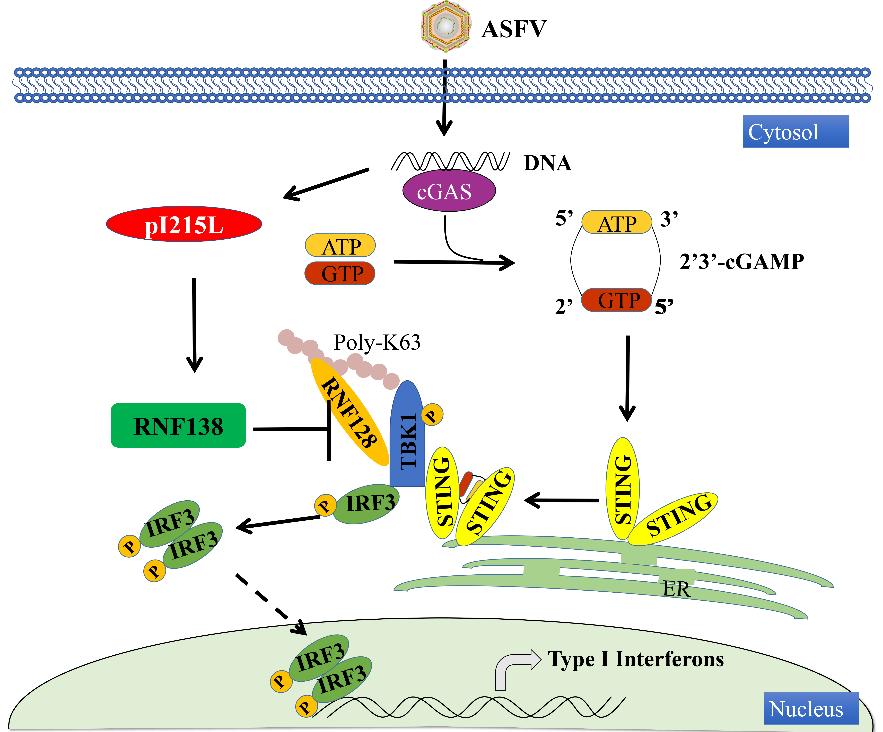
利用双荧光素酶报告基因系统筛选了ASFV 编码的102个蛋白对干扰素启动子活性的影响,科研人员发现ASFV编码的E2泛素结合酶(pI215L)对干扰素产生的抑制作用最为显著。利用siRNA敲低pI215L的表达显著抑制了ASFV的复制,但增强了ASFV诱导的IFN-β和ISG56的产生。利用免疫共沉淀联合质谱实验,我们发现与pI215L相互作用的E3泛素连接酶RNF138。pI215L通过招募RNF138并促进RNF138降解RNF128,进而抑制RNF128对TBK1的K63位泛素化修饰,最终抑制IFN-β产生。这些研究成果阐明了ASFV免疫逃逸的一种新机制,将为ASFV减毒疫苗的研制提供线索。
3. 发现非洲猪瘟病毒新的细胞凋亡诱导基因
细胞凋亡在病毒感染、复制和致病机制中起着非常重要的作用。2021年11月9日,哈尔滨兽医研究所发现一个非洲猪瘟病毒基因的新功能,并在其诱导细胞凋亡的机制上取得新进展。科研人员发现并证实非洲猪瘟病毒的pE199L基因是一个新的细胞凋亡相关基因,能够诱导线粒体依赖性的细胞凋亡,相关研究结果以“African swine fever virus pE199L induces mitochondrial-dependent apoptosis”为题,发表在《Viruses》杂志上。
ASFV感染猪后,临床特征表现为感染的组织内大量细胞死亡以及淋巴细胞枯竭,然而该病毒感染引起细胞死亡的分子机制目前仍不清楚。研究人员从ASFV编码的94个蛋白中筛选并鉴定出4个病毒蛋白能够引起细胞死,其中pE199L的作用最为显著。体外实验结果表明,在猪源细胞(CRL-2843)和人源细胞(HEK293T和HeLa)中,异源表达的pE199L可显著诱导细胞死亡,并且表现出明显的细胞凋亡特征,包括核皱缩、核DNA片段化、凋亡小体形成等。而在ASFV感染过程中,下调pE199L的表达可明显降低细胞的死亡。另外,pE199L的表达导致线粒体膜电位势能下降,细胞色素C释放以及凋亡相关激酶caspase-9和-3/7的激活,说明pE199L通过线粒体凋亡途径诱导细胞死亡。
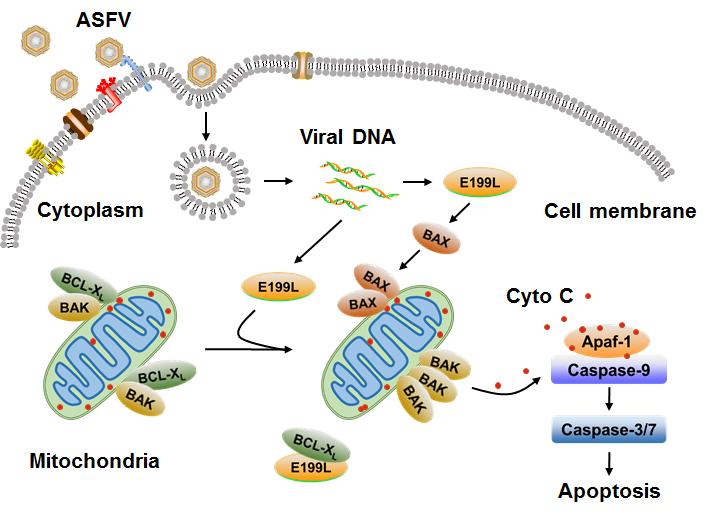
进一步研究发现,pE199L能够与BCL-2凋亡家族的抗凋亡成员(如BCL-XL、MCL-1、BCL-W、BCL-2A1)相互作用,并且与BAK竞争结合BCL-XL,从而促进BAK和BAX的活化,最终引起线粒体依赖性细胞凋亡。本研究为进一步了解非洲猪瘟病毒的致病机制提供了新的线索。
4. 发现了非洲猪瘟病毒pS273R蛋白抑制细胞焦亡的机制
病毒感染诱导炎症反应及其负调控机制一直是免疫学研究的前沿和重点。2021年11月15日,哈尔滨兽医研究所在非洲猪瘟病毒感染诱导炎症的负反馈机制研究上再次取得新进展。科研人员发现,非洲猪瘟病毒pS273R能够通过非典型切割Gasdermin D从而抑制细胞焦亡,相关研究结果以“African Swine Fever Virus pS273R Inhibits Pyroptosis by Non-canonically Cleaving Gasdermin D”为题,将发表在《Journal of Biological Chemistry》杂志上。
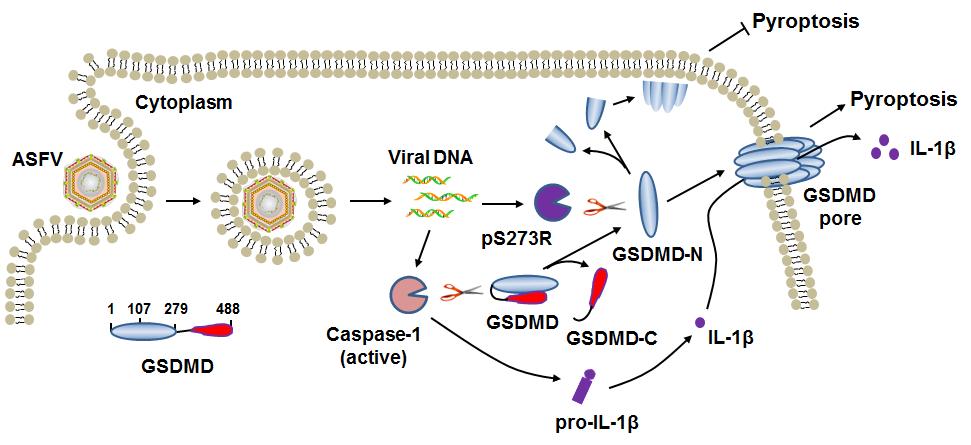
非洲猪瘟病毒基因组是一个长链双链DNA,编码超过150种蛋白质,其中一些蛋白质不仅参与病毒的生命周期,还参与病毒的免疫逃逸,但大部分蛋白的功能未知。初步研究发现ASFV编码的一种半胱氨酸蛋白酶pS273R能够结合细胞焦亡的执行蛋白Gasdermin D (GSDMD)。进一步的研究表明,非洲猪瘟病毒 pS273R依赖其酶活性特异性切割GSDMD的G107-A108位点,产生一个较短的GSDMD 氨基端片段(GSDMD-N1-107)。有趣的是,该片段与宿主细胞Caspase-1切割GSDMD产生的氨基端片段(GSDMD-N1-279)不同,GSDMD-N1-107不触发细胞焦亡或抑制非洲猪瘟病毒复制。进一步的鉴定结果显示 pS273R能够通过切割GSDMD阻碍细胞焦亡的发生,从而有利于病毒在宿主细胞内完成复制周期。这些研究成果揭示了一种未被认识到的非洲猪瘟病毒抑制细胞焦亡的机制,这突显了pS273R在炎症反应和非洲猪瘟病毒复制中的重要功能。
5. 发现影响非洲猪瘟病毒粒子形态的功能基因
非洲猪瘟病毒感染性颗粒的结构已经被解析,但是大多数病毒结构蛋白的定位及功能仍有待阐明。2021年11月17日,哈尔滨兽医研究所在非洲猪瘟病毒编码蛋白功能研究上取得新进展,科研人员首次发现非洲猪瘟病毒pH240R能够影响病毒粒子的组装从而降低子代病毒粒子的感染性,相关研究成果以“Deletion of the H240R Gene of African Swine Fever Virus Decreases Infectious Progeny Virus Production Due to Aberrant Virion Morphogenesis and Enhances the Inflammatory Cytokine Expression in Porcine Macrophages”为题,发表在《Journal of Virology》杂志上。
免疫电镜结果显示病毒的结构蛋白pH240R为衣壳蛋白,通过蛋白相互作用试验发现pH240R与主要衣壳蛋白p72存在相互作用。
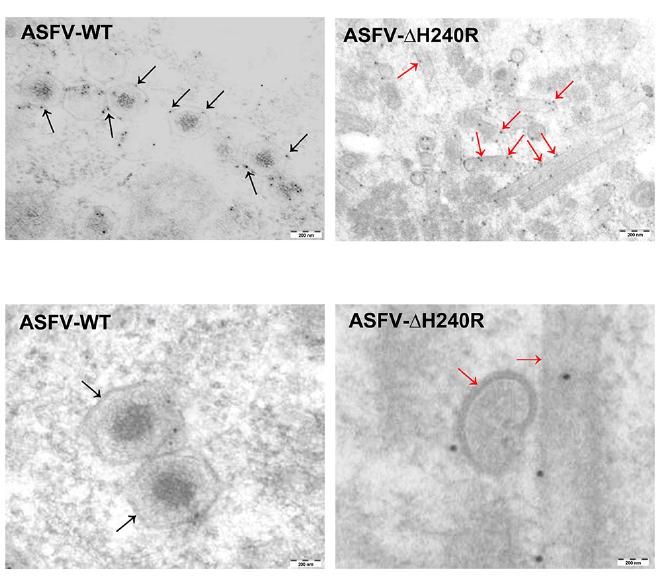
进一步研究发现,与ASFV HLJ/18毒株相比,ASFV-ΔH240R传染性子代病毒滴度降低了约100倍,而病毒基因组拷贝数没有明显变化,表明产生了大量无感染性的子代病毒。通过透射电镜观察,科研人员在ASFV-ΔH240R感染的原代猪肺泡巨噬细胞中发现了含有管状结构和双叶状结构的病毒粒子,占所有病毒粒子的近98%。pH240R不影响病毒细胞结合、内吞或排出,而是影响ASFV的组装。此外,研究人员还发现,与ASFV HLJ/18毒株相比,ASFV-ΔH240R感染原代猪肺泡巨噬细胞后,诱导了更高水平的炎性细胞因子TNF-α和IL-1β等的表达,提示H240R可能抑制了病毒感染诱导的炎症反应。该研究首次鉴定了一个新的衣壳蛋白,并为揭示非洲猪瘟感染机制提供了全新视角。
上一篇:哈兽研攻克种源性疫病“卡脖子”技术难题 支撑我国首批白羽肉鸡新品种(圣泽901)培育 下一篇:JVI │哈兽研新发现影响非洲猪瘟病毒粒子形态的基因